降血糖糖、改善β细胞功能和胰岛素抵抗,糖尿病治疗迎来新的曙光( 二 )
 文章插图
文章插图
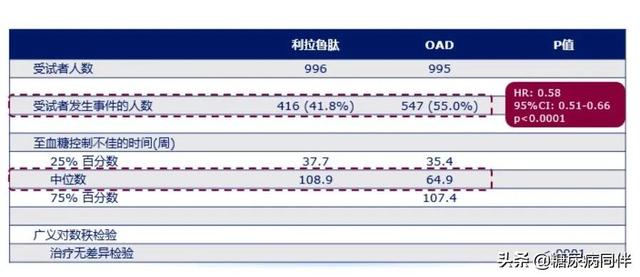
图2. LIRA-PRIME研究显示利拉鲁肽显著降低血糖控制不佳风险
T2DM远期心获益 & GLP-1RA循证证据+指南力荐
糖尿病治疗的远期目标是通过良好的代谢控制达到预防慢性并发症、提高患者生活质量和延长寿命的目的[11] 。 来自上海交通大学附属第一人民医院的彭永德教授指出 , T2DM患者中约1/3合并心血管疾病(CVD) , 其中85.8%的CVD被归类为动脉粥样硬化性心血管病(ASCVD)[12] 。 CVD是糖尿病患者死亡的最主要原因[13] 。 所以 , 应充分重视糖尿病患者心血管风险管理 。 多种危险因素管理可显著降低ASCVD相关心血管风险 。 而GLP-1RA具有降糖、降压、降脂减重 , 多重改善ASCVD相关危险因素 。 其机制可能为GLP-1RA多环节抑制动脉粥样硬化过程中的炎症反应、减轻氧化LDL(ox-LDL)诱导的血管内皮损伤、减少高血脂、糖尿病导致的动脉硬化斑块形成等作用[14-17] 。
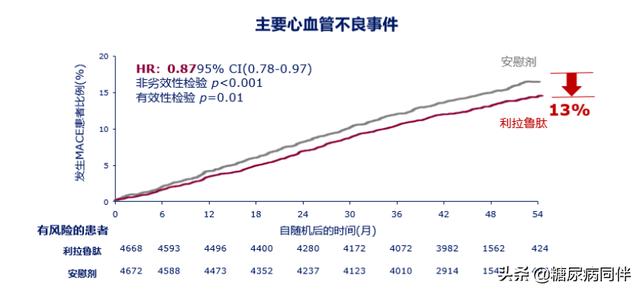
在CDS年会中贵州医科大学附属医院的时立新教授带我们重温了GLP-1RA利拉鲁肽的心血管结局研究(CVOT)LEADER 研究 。 此研究是一项多中心、国际、随机、双盲、安慰剂对照试验 。 结果显示 , 针对T2DM伴心血管高风险患者 , 中位随访3.8年 , 与安慰剂组相比 , 利拉鲁肽组可显著降低主要心血管不良事件风险(MACE)13%(非劣效检验P<0.001 , 优效性检验P=0.01);显著降低心血管死亡风险22%(P=0.007);显著降低全因死亡风险15%(P=0.02)[18](图3) 。
 文章插图
文章插图
图3. LEADER研究结果显示利拉鲁肽可以降低主要心血管不良事件
一系列LEADER研究事后分析显示[19] , 利拉鲁肽的心血管保护作用独立于基线血脂水平和他汀类药物的应用、独立于减少低血糖发生[20] 。 对糖尿病合并多血管区病变的患者同样有效[21] 。 利拉鲁肽是在患者充分应用已证明心血管获益药物应用基础上进一步降低了T2DM患者心血管残余风险 , 其证实糖尿病合并CVD或高风险患者在标准心血管药物治疗基础上使用利拉鲁肽可以进一步减少心血管事件发生风险 。 基于此项研究国家药品监督管理局(NMPA)正式批准了利拉鲁肽的心血管适应症 , 即用于降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件(心血管死亡、非致死性心肌梗死或非致死性卒中)风险 。 利拉鲁肽成为目前中国唯一具有心血管适应症的降糖药物 。
2020年发布的ADA最新糖尿病诊疗标准[22]、CDS年会刚刚发布的2020年CDS指南中 , 均对GLP-1RA等新型降糖药物进行了推荐更新:T2DM患者合并ASCVD或者心血管高风险 , 在二甲双胍治疗基础上无论HbA1c控制如何均应尽早启用GLP-1RA等已证实心血管获益的降糖药物 。 相比较2018ADA/EASD共识 , 新的指南增加了对于具有心血管高风险指标的人群的推荐 , 将降低心血管事件风险视为这类人群首要治疗目标 。
GLP-1RA的研发之路不断前行 , 来自北京大学人民医院的纪立农教授带我们认识了最新一代的GLP-1RA周制剂司美格鲁肽 。 虽同是周制剂 , 司美格鲁肽在降糖、减重方面优于艾塞那肽周制剂和度拉糖肽[23,24];同时司美格鲁肽在其CVOT研究中观察到显著的心血管获益[25] ,在中国受试者进行的临床研究中降低HbA1c达1.8% , 提高HbA1c(<7%)达标率达86%[26] , 是适合中国T2DM的GLP-1RA之选 。
总结
【降血糖糖、改善β细胞功能和胰岛素抵抗,糖尿病治疗迎来新的曙光】随着临床研究、循证证据的不断涌现 , T2DM治疗的理念不断完善 。 本届CDS年会中展示了GLP-1RA等新型降糖药物的众多证据 。 GLP-1RA同时具有降糖、改善β细胞功能和胰岛素抵抗、改善心血管危险因素 , 并具有远期心血管获益等作用 , 可以满足临床治疗的需求所在 , 得到国内外各大指南的一致推荐 。 最新发表的2020CDS指南亦推荐T2DM患者合并ASCVD或者心血管高风险 , 在二甲双胍治疗基础上无论HbA1c控制如何均应尽早启用GLP-1RA等已证实心血管获益的降糖药物 。 最新一代GLP-1RA周制剂司美格鲁肽循证证据完善 , 临床应用未来可期 。
推荐阅读
- 糖尿病的五个表现,你了解吗?若能早点掌握,或许可以稳住血糖值
- 血糖偏高时,脚上可能出现这三种现象,你或许还没注意到
- 打破传统治疗标准!拉罗替尼挑战转移性非小细胞肺癌的一线治疗
- 发现有口臭?可能是消化道出问题了,送你3个好办法,有效改善
- 最简血糖值记忆法345678、7111、9111
- 这4种家常菜,多吃血糖或许会“飙升”,糖友们要记住,尽量少碰
- 八宝丹,国家保密配方,改善乙肝患者症状、肝功能指标,消退黄疸
- 细胞|国内首个!浦东企业开启肿瘤免疫治疗新征程
- 千古“降痰”第一方!上清肺痰,下补阳气,改善痰多咳嗽
- 全球首次确认!母亲生产时宫颈癌细胞通过羊水转移致婴儿肺癌



![[坦言]收入提高了?滴滴司机坦言:因为平台这波操作,现在收入](/renwen/images/defaultpic.gif)













