2020胰腺癌年度热点回顾( 二 )
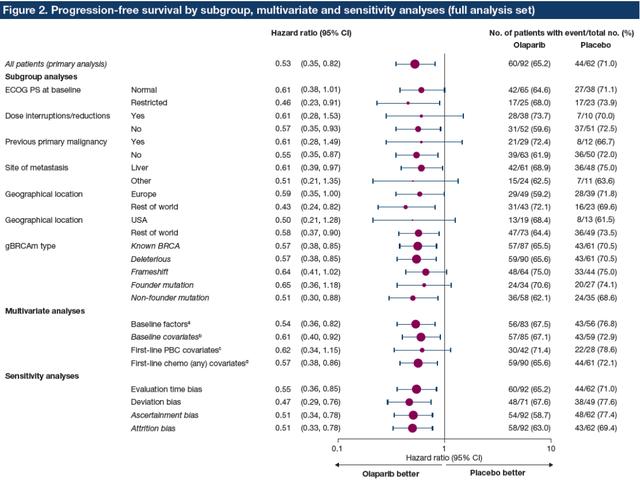
III期POLO试验显示 , 最终研究显示:所有亚组、敏感性和多变量分析均表明 , 与安慰剂相比 , 奥拉帕利维持治疗降低疾病进展风险 , 与主要终点一致 。 无论临床因素、地理位置或其他基线因素如何 , 与安慰剂相比 , 奥拉帕利维持治疗在铂类药物化疗期间未发生进展的携带生殖系BRCA1和/或BRCA2突变的转移性胰腺癌患者中 , 显示了一致、显著的PFS获益 , 并且没有证据表明POLO研究存在常见类型的研究设计偏倚 。
 文章插图
文章插图
热点3:胰腺癌的系统治疗有哪些进展?
? ESPAC-4研究:吉西他滨联合卡培他滨对比吉西他滨单药辅助治疗胰腺导管腺癌的多中心、国际、开放性随机对照III期临床研究:5年随访结果[4](2020 ASCO)
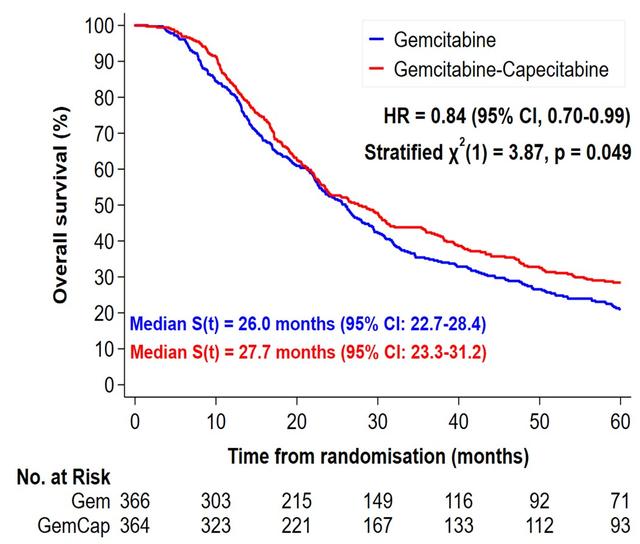
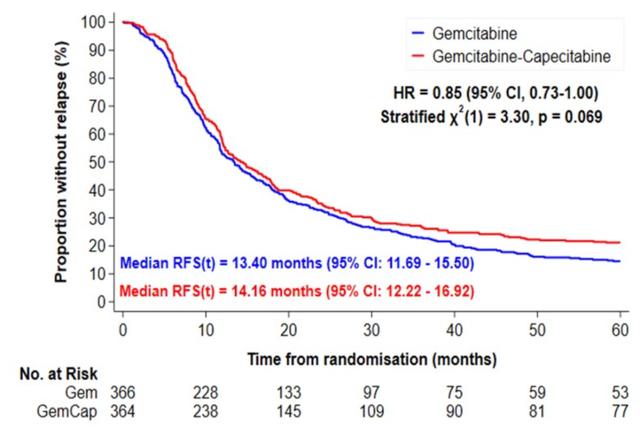
ESPAC-4研究表明 , 吉西他滨联合卡培他滨相比于吉西他滨单药辅助治疗胰腺导管腺癌患者显著提高了生存率[5] , 2020年ASCO上公布了ESPAC-4试验的长期生存结果 。 截至2020年2月24日 , 中位随访60个月 , 总死亡病例数531例 , 吉西他滨单药组280例 , 吉西他滨+卡培他滨组251例 。 吉西他滨+卡培他滨组的中位OS长于吉西他滨单药组 , 且具有统计学差异(27.7个月 vs 26.0个月 , P=0.049);吉西他滨+卡培他滨组的中位RFS长于吉西他滨单药组 , 但二者无统计学差异(14.16月 vs 13.40月 , P=0.069) 。
 文章插图
文章插图
 文章插图
文章插图
? 白蛋白紫杉醇联合吉西他滨与吉西他滨单药辅助治疗胰腺癌的III期研究(APACT研究):更新的总生存和地域分析结果[6](2020 ASCO)
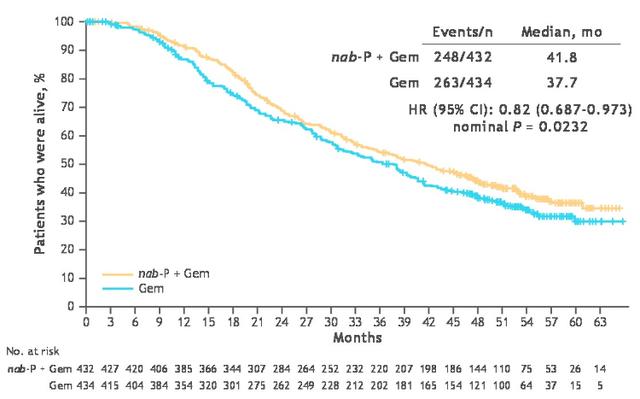
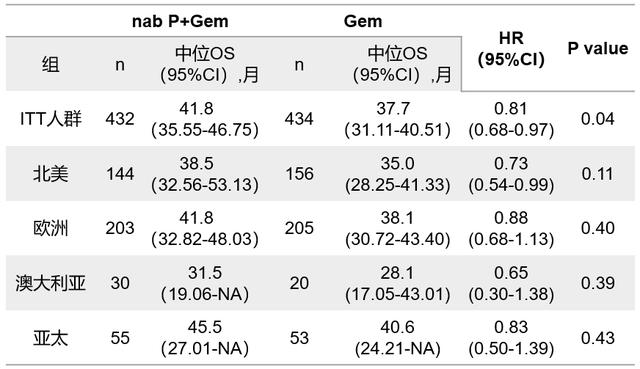
【2020胰腺癌年度热点回顾】APACT研究虽然并未达到预设的主要终点DFS , 但次要终点OS在联合组有获益趋势(40.5个月 vs 36.2个月 , P=0.045) 。 2020年ASCO上报道了APACT研究意向治疗人群的最新总生存结果 , 并按不同地域分析了结果 。 白蛋白紫杉醇联合吉西他滨组和吉西他滨单药组的中位OS分别为41.8个月和37.7个月(P=0.0232) , 4年OS率分别为44%和38% 。 此外对欧洲、北美、亚太和澳大利亚不同地域分析显示 , 白蛋白紫杉醇联合吉西他滨组的OS在数值上更长:
 文章插图
文章插图
 文章插图
文章插图
? 脂质体伊立替康+5-氟尿嘧啶/亚叶酸+奥沙利铂(NALIRIFOX)一线治疗胰腺导管腺癌患者:一项I/II期研究的长期随访结果[7](2020 WCGIC)
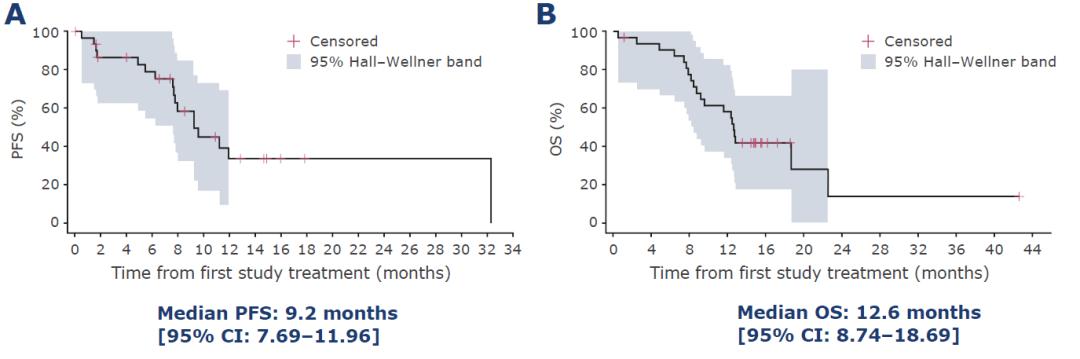
一项评估脂质体伊立替康+5-氟尿嘧啶/亚叶酸+奥沙利铂(NALIRIFOX)一线治疗胰腺导管腺癌患者的I/II期研究在剂量探索部分通过传统3+3设计爬坡确定安全剂量:伊立替康脂质体50mg/m、5-FU2400mg/m、LV400mg/m和OX60mg/m2 2 2 2;在合并剂量扩展人群后共32例患者 , 长期随访结果表明在合并人群中 , NALIRIFOX方案治疗胰腺癌的mPFS=9.2个月 , mOS=12.6个月 , ORR达34.4% , DCR达71.9% 。 此项研究表明NALIRIFOX方案治疗胰腺癌安全有效 , III期临床研究NAPOLI-3正在开展中 。
 文章插图
文章插图
热点4:胰腺癌目前存在哪些具有潜力的生物标志物可能用于指导胰腺癌的治疗?
? KRAS与胰腺癌(2020 ASCO)
KRAS在胰腺癌起始、进展和转移中发挥着显著的作用 , 但是目前仍缺乏特异性靶向KRAS的有效药物 。 80-90%的胰腺癌患者存在KRAS突变 , 75%的胰腺癌正是由于这种极高突变率导致不能找到可接受治疗的靶点 。 KRAS野生型胰腺癌靶分子通路改变富集研究应用分子检测平台(NGS、WTS、IHC、MCP等)检测KRAS野生型PC中分子靶向靶点分布的情况.结果表明相比KRAS突变型胰腺癌 , 野生型有更丰富的靶点异常(诸如:BRAF、ALK、ROS1、NRG1、MSI-H等) , 提示可能获益于靶向治疗 , 此外KRAS野生型有更高的TMB和MSI-H , 伴低成纤维细胞丰度和被活化的先天免疫微环境状态 , 都提示着可采取独特的免疫治疗策略[8] 。
推荐阅读
- 喜讯!松滋市中医院在2020年度中医中药荆楚行中医适宜技术竞赛中获奖
- 干货|全球上市的十大PD-1/L1用药信息大盘点!2020版
- 「ITC2020」妊娠期亚临床甲状腺功能减退症与子代神经智力发育
- 国寿核保之声|得了胰腺炎该如何买保险
- 晨会交班小评比 标准规范大内涵——南充市中心医院护理部举办2020年晨交班比赛
- 2020最新获批的PD-1/L1疗法汇总?(囊括13类癌症)
- 贾冰出席星锐榜盛典群星璀璨 获“年度最具热度男演员” 实至名归
- 五莲县人民医院被省卫健委命名为2020年度优质服务单位
- 2020年广东省继续教育项目“针推技术临床运用与进展培训班”暨广东省针灸学会针推结合专业委员会换届会议在广州成功举办
- 【2020健康北京科普大赛获奖作品】蚊子叮咬后的正确止痒方式










![[乐居财经]黄红云“封赏”金科2100名基层员工](https://imgcdn.toutiaoyule.com/20200415/20200415084109976199a_t.jpeg)






