|磷:尿液、生命之源与致命毒药
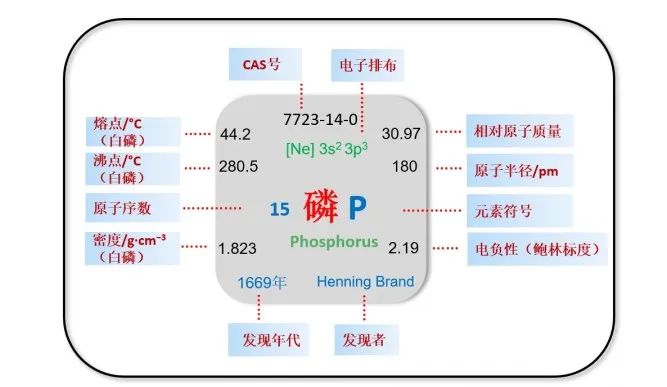
本文图片
作为人类首个明确记录了发现过程的常见元素 , 磷的故事充满了戏剧性 。 我们为何对磷又爱又怕?它究竟是生命不可或缺的卫士还是令人闻之色变的魔鬼?
撰文 | 李研
责编 | 刘睿 李珊珊
磷的发现极具传奇色彩 。
1669年的一个夜晚 , 在德国汉堡圣米迦勒教堂(St. Michael's Church)的地下室里 , 一位名叫波兰特(Henning Brand)的炼金术士正试图从尿液中获取“哲人石” 。 和当时其他笃信炼金术的人一样 , 波兰特热衷于寻找这种能够将廉价金属变为贵重黄金的神奇物质 。 至于为什么匪夷所思地选择了尿液 , 据说是因为他觉得人体本身就很神奇 , 从嘴巴吃进去的跟排泄出来的物质完全不一样 , 而尿作为人体液的一种 , 颜色又和黄金有那么点接近 , 没准就是成功的关键呢 。 在当晚的实验中 , 他将砂、木炭、石灰等和尿混合 , 加热蒸馏 。 这一次 , 他的虔诚之心似乎得到了回报 , 一种带有蜡状白色固体意外出现了 。 这种物质在幽暗的地下室里 , 竟然不需加热就能发出美丽的光 。 注1
波兰特马上意识到自己发现了不寻常的东西 。 他最初把这种物质叫做kalte feuer(德文意为冷火) , 后来又称之为“phosphorus” 。 这个名字由”phos”(光)和”phorus”(承载者)组成 , 意为“光的载体“ 。
世界上知名的油画不可胜数 , 但约瑟夫·怀特(Joseph Wright)在1771年完成的《炼金术士发现磷》是屈指可数的以化学新发现为素材的名画 。 画家用生动而夸张的笔触重现了科学史上那个重要的时刻——波兰特目光炯炯 , 虔诚地注视着蒸馏瓶中醒目的光辉 。
本文图片
The Alchemist Discovering Phosphorus (1771) by Joseph Wright 。 这幅画的完整标题是:“寻找哲人石的炼金术士发现了磷 , 他在祈祷自己的操作可以成功 , 就像古代化学占星术士的笔记一样 。 ”
图源:Wikipedia
该发现使波兰特不仅成为发现磷元素的第一人 , 还无意间成为化学史上有记录的第一个发现新元素的人 。 之前已知的化学元素(如金、银、铜、铁等)因为很早就应用在生产和生活中 , 并没有明确史料记载它们的发现者 。
然而 , 那时的人们对化学元素的概念还一无所知 , 波兰特本人也没有意识到自己发现的科学意义 。 作为一个还有些商业头脑的人 , 他起初打算严守机密 , 期待从这种奇特发光物质中获利 。 遗憾的是 , 这种发光物质并不是他设想的能够点石成金的“哲人石” , 而且由于具有强烈的臭味又极为易燃 , 也难以取代蜡烛用于室内照明 , 似乎没有半点用处 。 于是 , 他只能靠偶尔透露这种发光物质的一些细节来换点小钱 。 消息不胫而走 , 德累斯顿一位名叫克拉夫特(Daniel Kraft )的商人成功说服波兰特以很低的价钱出售了从尿液制磷的方法 , 而后转手在欧洲广泛传播 , 获利颇丰 。 只是不知道波兰特得知后会作何感想 。
在波兰特发现磷大约10年后 , 作为近代化学的重要开创者 , 英国化学家波义尔(Robert Boyle , 1627-1691)借助从德国获取的消息 , 成功复制了从尿液中提取磷的实验 。 随后他将磷的制备方法以及磷的一些性质公之于众 。
在波兰特发现磷50年后 , 一位名叫约翰·亨欣(Johann Thomas Hensing)的德国药剂师又在人脑中提取出同样的物质 。 因为大脑中含有磷 , 18世纪初的一些人曾将磷视为可以补脑的保健品 。 然而 , 随意服用含磷药物不仅不能补脑 , 还往往会导致磷中毒 。
波兰特发现磷100年后 , 瑞典科学家又发现磷还广泛存在于人和动物骨骼中 , 将硫酸和骨灰放在一起加热也可以得到磷 。 这让磷的获取变得更加容易 。
随着元素概念的发展 , 到了1796年 , 法国著名化学家拉瓦锡(Antoine-Laurent de Lavoisier , 1743-1794)终于认识到波兰特提取的发光物质是一种元素 。 Phosphorus这一名字被沿用 , 磷(元素符号P)自此正式成为元素家族中的一员 。
多变的磷
波兰特当年发现的磷是白色蜡状固体 , 但磷原子通过不同的排列方式 , 还可以变身为红色粉末 , 或者带有金属光泽的黑色固体等多种形态 。 化学家把这些由同种元素组成 , 但化学和物理性质并不相同的物质称为同素异形体 。
磷常见的同素异形体包括白磷、红磷和黑磷等几种 。
本文图片
白磷(左)、红磷(中)和黑磷(右)的形态及分子结构
图源:Wikipedia
白磷是一种白色或浅黄色半透明态的固体 , 分子式为P4 , 其中四个磷原子通过六根P-P键形成正四面体结构 。 分子结构具有很强的张力 , 导致白磷的反应活性很高 , 在室温下就可以与空气中的氧气反应 , 并发出冷光 。
推荐阅读
- 科学|世界3大未解之谜:生命起源、地球内核、宇宙之谜,该如何解释?
- 鬼才狗仔|皮肤被冻伤,处理能挽救生命!医生告诉你如何防治
- 科学|有些星球可能比地球更适宜生命繁衍?科学家一下发现24颗候选者
- 杨丽萍 |舞蹈家杨丽萍:跳舞是我生命的需要
- 外星生命|距离地球最远的探测器,携带人类生殖器官图像,飞了整整41年!
- 外星生命|距离地球最远的探测器,飞了整整41年,看完令人绝望!
- 买单|你穿的每一条牛仔裤, 都是在用生命买单
- 科学|“基因魔剪”将生命科学带入一个新时代,如何善用还需全社会共同努力
- 诺贝尔化学奖|科普:重写生命密码的工具——解读2020年诺贝尔化学奖成果
- 剪刀|科普:重写生命密码的工具——解读2020年诺贝尔化学奖成果